日本で抗がん剤といえば、化学療法剤とか、殺細胞剤と呼ばれる、正常細胞もがん細胞も区別なく、分裂中(増殖中)の細胞の遺伝子に傷をつけるタイプのものがほとんどです。欧米では、殺細胞剤の使用は主流ではなくなりつつあり、圧倒的にシェアが高いのが分子標的薬とよばれるものです。
がんのほとんどは上皮組織由来です。従い、分子標的薬の代表的なものは、上皮組織特有の細胞増殖に関係する物質を標的にしています。そのため、正常な上皮組織にも影響は与えますが、免疫細胞は上皮組織ではないため、分子標的薬の直接の影響は受けません。ただし血液のがんを標的とする分子標的薬は、免疫細胞に影響します。
がん、といっても、活発に増殖しない、また、それほど転移しないものであれば、危険度は低いわけです。「危険ながん」は成長速度が早く、転移する傾向が強いものです。増殖因子のレセプターを異常に大量にもつ(過剰発現する)がん細胞は、「危険ながん細胞」と考えられ、増殖因子のレセプターをブロックすることで、危険ながんの増殖を抑える、という分子標的薬が開発の中心です。
標準治療だけでは完治せず、再発や転移を繰り返す予後の悪いがんが、過剰発現している代表的な細胞表面レセプターとして、EGFRとHER2が知られており、両方を発現しているものもあります。他にも数十種類が知られており、それぞれが、分子標的薬の開発対象になってきましたが、その中でも、特に重要なEGFRとHER2を標的とするものに集中しています。分子標的薬は、抗体を利用する抗体医薬品と、低分子の化学物質でつくられる低分子分子標的薬があり、それぞれに、EGFRを標的とするもの、HER2を標的とするもの、両方を標的とするものなどがあります。
EGFRと表記されるアンテナを過剰発現しているがん細胞は、隣接する正常組織を盛んに浸食し、どんどんその場で大きくなり、手術で取り除いたと思っても、近傍に散っていた分散がんが増殖し、再発や近傍への転移をしやすい傾向があります。
低分子分子標的薬のゲフィニチブ(商品名:イレッサ)は、EGFと呼ばれる成長因子の一種が惹き起こす細胞分裂のプロセスを、細胞の内部まで入り込んでブロックします。低分子分子標的薬は、抗体医薬品よりも細胞分裂を抑えるパワーは強いのですが、特段、NK細胞を刺激することはありません。
1.細胞表面に突き出したレセプターで、細胞増殖因子を受け取ります。
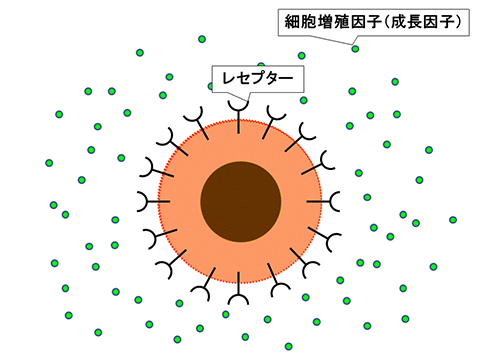
2.レセプターが細胞増殖因子を受け取ると、細胞内に変化を起こす信号を送ります。
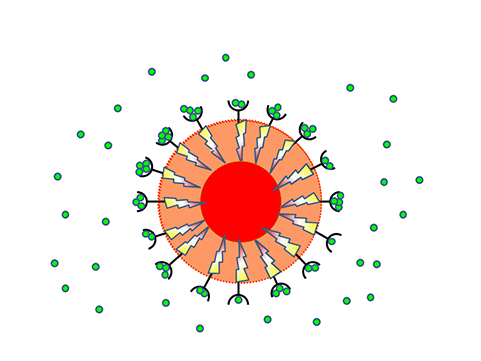
3.ゲフィニチブは細胞の内部入り込み、レセプターの増殖信号をブロックすると考えられています。
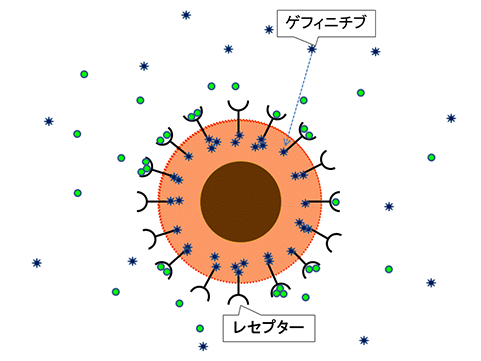
ゲフィニチブ(商品名:イレッサ)は、非小細胞性の肺がんに適用が認められましたが、原理からすれば、部位の問題ではなく、EGFR(EGFレセプター、EGFを受け止めるアンテナ)を過剰発現しているがん細胞に対して、より有効と考えられます。
他に、エルロチニブ(商品名:タルセバ)、やラパチニブ(商品名:タイケルブ)などがあります。また、EGFRを標的とする抗体医薬品に、セツキシマブ(商品名:アービタックス)などがあります。
なお、ラパニチブはEGFR とHER2の両系統の増殖信号をブロックすると考えられています。
また、セツキシマブは、ADCC活性を作用機序のひとつとすると考えられていますが、保険診療においては、EGFR系の増殖信号をブロックするものとみなされています。
EGFレセプターが過剰発現となる割合
(国立がんセンター) |
| 腫瘍の種類 |
EGFR過剰発現の割合 |
| 肺がんの一部 |
40-80% |
| 前立腺がん |
40-80% |
| 胃がん |
33-74% |
| 乳がん |
14-91% |
| 大腸がん |
25-77% |
| 膵臓がん |
30-50% |
| 卵巣がん |
35-70% |
同じEGFRの仲間で、HER2と呼ばれるアンテナもあり、これを過剰発現するがんの場合、盛んに遠隔転移する傾向があります。
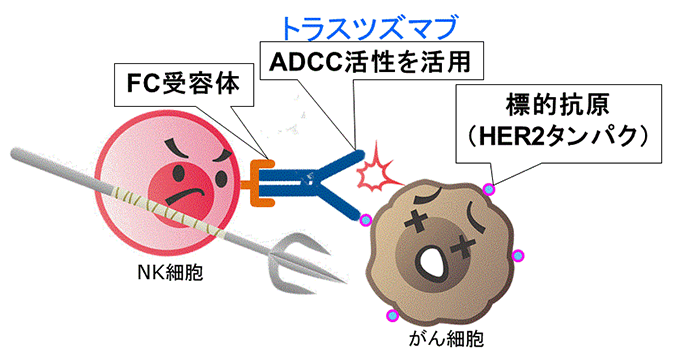
抗体医薬品の代表格トラスツズマブ(商品名:ハーセプチン)は、HER2に結合するものです。細胞増殖を抑えるパワーは低分子分子標的薬には敵いません。トラスツズマブもまた、乳がんを対象に保険適用になりましたが、やはり本来は部位に関係なく、がん細胞がハーセプチンの標的となるHER2を過剰発現(HER2抗原強陽性)しているがんに対して、使用を検討すべきものと考えられます。他にも、ペルツズマブ(商品名:パージェタ)がHER2を標的とするものです。
EGFレセプター2型(HER2)抗原が
強陽性(過剰発現)となる割合 |
| 腫瘍の種類 |
症例数 |
HER2タンパク過剰発現の割合 |
| 乳がん |
2111 |
17-37% |
| 卵巣がん |
73 |
32% |
| 胃がん |
459 |
12-55% |
| 非小細胞がん |
207 |
27-56% |
| 間葉がん |
94 |
37% |
| 膀胱がん |
141 |
36% |
| 食道がん |
25 |
60-73% |
| 唾液腺腫瘍 |
27 |
32-62% |
| Hynes NE et al:Biochem Biophys Acta 1198,165,1994 |
なお、分子標的薬には、細胞増殖に関係する物質以外を標的とするものもあります。
代表的なものは、リツキシマブ(商品名:リツキサン)です。これは、B細胞に多く存在するCD20という物質を標的とします。CD20は、正常なB細胞にも沢山、存在するため、大量の抗体(リツキサン)が正常細胞に吸着されます。そのため、投与量が多く、値段が高いのがネックです。また、この抗体は、B細胞ががん化したもの、悪性リンパ腫B型専用のものです。
他にも、血管新生阻害というタイプがあります。腫瘍組織は、数ミリ程度まで大きくなると、組織内部に血液が循環せず、成長できなくなります。そこで、腫瘍組織は自ら血管網を形成しようとします。この血管新生を阻害すれば、腫瘍組織の巨大化を防げる、と言う考え方です。
現在、開発中の新薬については、細胞増殖に関係するものに集中しています。EGFレセプターやHER2抗原といった、既存品が存在する同一標的に対し、特性の異なる複数の抗体医薬品が開発中です。また、一部にマウス由来の構造を残している抗体を完全にヒト型に変更したもの、最初からヒト抗体として開発されているものなどもあります。
分子標的薬は、がん細胞の増殖にブレーキをかけるだけで、原則、傷害はしません。
実際に、臨床試験のエビデンスとしては、せいぜい2~3ヶ月の延命効果を示しているに過ぎません。統計数値だけをみれば、分子標的薬は、それほど威力がないように、一見、みえてしまいます。がん専門医も、それほど切れ味はない、という印象をもつ方が多いようです。ただし、これには使い方の問題もあると考えております。
たとえば、強い増殖抑制作用をもつ分子標的薬を単独投与すると、薬剤自体に、がん細胞を殺す機能はないにもかかわらず、確率は低いながらも、腫瘍が消滅し、その後再発しない著効例がでることがあります。がん患者様体内にも、1000億個レベルのNK細胞が存在するのですが、活性が低下しているために、がん細胞を攻撃するスピードが落ちています。つまり、がん細胞を殺していないのではなく、がん細胞の増殖スピードに一方的に押されている、ということです。そこへ、しばらくの期間、分子標的薬が強力にがん細胞の増殖にブレーキをかければ、活性が低下したNK細胞によるゆっくりとした攻撃でも、腫瘍が消滅することは考えられます。残念ながら、そこまで分子標的薬の効果が持続せず、がんが全滅する前に増殖に転じるケースの方が多く、また、日本では、殺細胞剤を分子標的薬と併用することが多いため、肝心のNK細胞が殺細胞剤にやられてしまい、著効にはなりにくい状況となります。ANK療法を実施する場合、免疫系がん治療薬である分子標的薬を、殺細胞性化学療法とは一緒に投与せずに、ANK療法と同時に併用することで、本来の効果を発揮できるような治療設計を行います。
分子標的薬の中でも、抗体医薬品と呼ばれるものの多くは、増殖抑制作用に加えてADCC活性(抗体依存性細胞傷害活性)とよばれる機能をもちます。これは、体内のNK細胞が、がん細胞を攻撃する効率を高める作用のことです。世界の抗がん剤開発は、今や、がん細胞の増殖を暫くとめるだけで、その間に、NK細胞ががん細胞を狙い撃ちするのを助けることに懸けているのです。
残念ながら、日本の保険診療では、分子標的薬はほとんどの場合、殺細胞剤と併用されることが多く、しかも、免疫抑制剤であるステロイドを一緒に投与するため、折角のADCC活性を作用機序としながら、肝心のNK細胞が叩かれているため、本来の威力を発揮できません。





